Ritme Kompleks Kimia
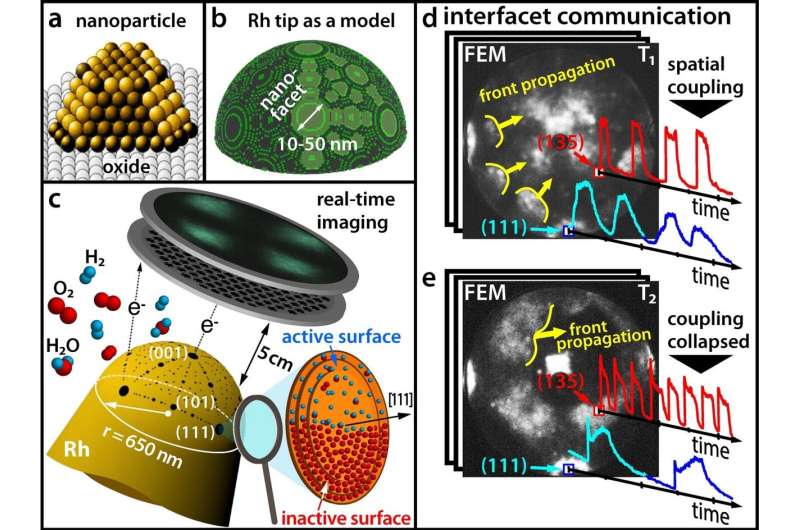
(A) Terminologi modern terdiri dari nanopartikel; (B) Ujung rodium sebagai model nanopartikel; (C) Melacak reaksi kimia dalam waktu nyata menggunakan mikroskop emisi medan (d) Pada suhu yang lebih rendah, sisi yang berbeda berosilasi secara serempak (e) Pada suhu yang lebih tinggi, sinkronisasi terputus. Kredit: Universitas Teknologi Wina
Sebagian besar bahan kimia komersial diproduksi dengan menggunakan katalis. Biasanya, katalis ini terdiri dari nanopartikel logam kecil yang ditempatkan pada penyangga pengoksidasi. Mirip dengan potongan berlian, yang permukaannya terdiri dari permukaan yang diarahkan ke berbagai arah, nanopartikel katalitik juga memiliki aspek kristalin yang berbeda – dan aspek ini dapat memiliki sifat kimia yang berbeda.
Sampai saat ini perbedaan tersebut masih sering diabaikan dalam penelitian motivasi karena sangat sulit untuk memperoleh informasi tentangnya Bahan kimia Reaksi itu sendiri dan tentang struktur permukaan katalis. Di TU Wien (Wina), ini sekarang dicapai dengan menggabungkan metode mikroskopis yang berbeda: dengan bantuan mikroskop elektron medan dan mikroskop ion medan, menjadi mungkin untuk memvisualisasikan oksidasi hidrogen pada Rhodium Nanopartikel real-time dengan resolusi nanometer. Ini mengungkapkan efek mengejutkan yang harus diperhitungkan saat mencari rangsangan yang lebih baik di masa depan. Hasilnya sekarang disajikan dalam jurnal ilmiah Ilmu.
Ritme reaksi kimia
“Dalam beberapa interaksi chimical“Katalis dapat secara berkala beralih antara keadaan aktif dan tidak aktif,” kata Profesor Günther Rubrichter dari Institut Kimia Material di TU Wien. Dia dianugerahi Hadiah Nobel Kimia untuk penemuan ini pada tahun 2007. “
Ini juga kasusnya dengan Nanopartikel rhodium, Yang digunakan sebagai katalis untuk oksidasi hidrogen – dasar dari setiap sel bahan bakar. Dalam kondisi tertentu, file Partikel nano Bisa berayun di antara keadaan mana Molekul oksigen Di permukaan partikel dan keadaan di mana hidrogen terikat.
Oksigen gabungan mengubah perilaku permukaan
“Saat partikel rodium terpapar atmosfer Oksigen Dan hidrogen, molekul oksigen dibagi menjadi Atom individu Di permukaan rhodium. Atom oksigen ini dapat bermigrasi di bawah lapisan rhodium atas dan berakumulasi sebagai oksigen di bawah permukaan di sana, ”jelas Profesor Yuri Souchorsky, penulis pertama studi tersebut.
Dengan berinteraksi dengan hidrogen, atom oksigen yang tersimpan kemudian dapat dikeluarkan kembali dan berinteraksi dengan atom hidrogen. Lalu masih ada ruang untuk lebih banyak lagi Atom oksigen Di dalam partikel rhodium dan siklus dimulai lagi. “Mekanisme umpan balik mengontrol frekuensi osilasi,” kata Yuri Souchorsky.
Hingga saat ini, diperkirakan bahwa osilasi kimiawi ini selalu terjadi secara bersamaan pada ritme yang sama di seluruh partikel nano. Bagaimanapun, proses kimia di berbagai sisi permukaan nanopartikel terkait secara spasial, karena atom hidrogen dapat dengan mudah berpindah dari satu sisi ke sisi yang berdekatan.
Namun, hasil kelompok penelitian Profesor Günter Rubrichter dan Profesor Yuri Souchorsky menunjukkan bahwa hal-hal sebenarnya lebih rumit: Dalam kondisi tertentu, kopling spasial dinaikkan dan sisi-sisi yang berdekatan tiba-tiba berosilasi pada frekuensi yang sangat berbeda – dan di beberapa wilayah di partikel nano, gelombang “kimiawi” yang berosilasi ini tidak menyebar sama sekali.
“Ini bisa dijelaskan pada skala atom,” kata Yuri Souchorsky. Di bawah pengaruh oksigen, barisan atom rodium yang menonjol bisa muncul dari permukaan yang halus. Deretan atom ini dapat bertindak sebagai semacam “pemecah gelombang” dan menghalangi transfer atom hidrogen dari salah satunya Wajah Ke yang lain – dial terpisah.
Jika ini masalahnya, masing-masing sisi dapat membentuk osilasi dengan frekuensi yang berbeda. “Di sisi yang berbeda, atom rodium tersusun berbeda di permukaan,” kata Günther Rupprechter. “Itulah mengapa penggabungan oksigen di bawah sisi berbeda dari partikel rodium juga dilakukan pada kecepatan yang berbeda, dan karena itu osilasi frekuensi yang berbeda mengarah pada aspek yang berbeda secara kristal.”
Ujung belahan sebagai model nanopartikel
Kunci untuk memecahkan perilaku kimiawi yang kompleks ini adalah dengan menggunakan ujung rodium tipis sebagai model untuk nanopartikel katalitik. Medan listrik diterapkan, dan karena efek penerowongan mekanis kuantum, elektron dapat meninggalkan ujungnya. Elektron ini dipercepat pada Medan listrik Dan mengenai layar, di mana gambar proyeksi anggota badan dengan resolusi sekitar 2 nm kemudian dibuat.
Tidak seperti mikroskop, di mana situs permukaan dipindai satu per satu, pencitraan paralel seperti itu menggambarkan keseluruhan. Permukaan – penampilan luar Atom Bersamaan – jika tidak, tidak mungkin untuk mengamati sinkronisasi dan asinkronisasi osilasi.
Wawasan baru ke dalam interaksi aspek individu nanopartikel sekarang dapat mengarah pada katalis yang lebih kuat dan memberikan wawasan atom yang mendalam ke dalam mekanisme kinetika interaksi nonlinier, pembentukan pola dan kopling spasial.
Y. Suchorski et al, Solusi osilasi multi-frekuensi dan interkoneksi skala nano dalam stimulasi partikel tunggal, Ilmu (2021). DOI: 10.1126 / science.abf8107
Pengenalan
Universitas Teknologi Wina
kutipan: Nanoparticles: The Complex Rhythm of Chemistry (2021, May 21) Diperoleh 21 Mei 2021 dari https://phys.org/news/2021-05-nanoparticles-complex-rhythm-chemistry.html
Dokumen ini memiliki hak cipta. Terlepas dari perlakuan yang adil untuk tujuan studi atau penelitian pribadi, tidak ada bagian yang boleh diperbanyak tanpa izin tertulis. Konten tersebut disediakan untuk tujuan informasional saja.
